Candidose intestinale : comprendre les causes, les signes et les solutions naturelles
Candidose intestinale : Candida albicans inoffensif… en temps normal
La candidose intestinale correspond à une prolifération excessive de levures du genre Candida dans le tube digestif¹. Ce déséquilibre fongique survient souvent lorsque la diversité bactérienne protectrice diminue. Les manifestations restent habituellement localisées au niveau intestinal. Toutefois, dans des cas très rares, chez des personnes sévèrement immunodéprimées, le Candida peut franchir la barrière intestinale².
Les agents responsables
Le genre Candida regroupe près de 200 espèces, dont une vingtaine peuvent être associées à des troubles chez l’humain³. Les cinq plus fréquemment identifiées sont : Candida albicans, Candida glabrata, Candida parapsilosis, Candida tropicalis et Candida krusei. À elle seule, Candida. albicans représente jusqu’à 80 % des souches détectées dans le microbiote intestinal.
Microbiote déréglé : Candida, coupable ?
Candida albicans est naturellement présent en petite quantité sur la muqueuse digestive. En cas de baisse de la concurrence bactérienne, de modification du pH ou de déshydratation locale, Candida peut se transformer. Il développe alors des filaments capables d’adhérer à la paroi intestinale, favorisant ainsi sa persistance et son expansion¹.
Pourquoi Candida prolifère-t-il ?
Facteurs alimentaires
Une alimentation riche en sucres rapides constitue un environnement favorable à la croissance des levures⁵. En excès, ces apports peuvent contribuer à déséquilibrer le microbiote intestinal.
Médicaments
La prise prolongée d’antibiotiques peut réduire significativement la flore bactérienne bénéfique, modifiant ainsi l’équilibre du microbiote⁷.
Stress chronique
Le stress chronique libère du cortisol, une hormone qui peut altérer la perméabilité intestinale et influencer l’équilibre microbien et immunitaire.
Facteurs environnementaux et physiologiques
Certains polluants, modes de vie sédentaires ou troubles métaboliques peuvent perturber l’écosystème intestinal, contribuant ainsi à une diversité bactérienne moindre.
Candidose intestinale et hyperperméabilité
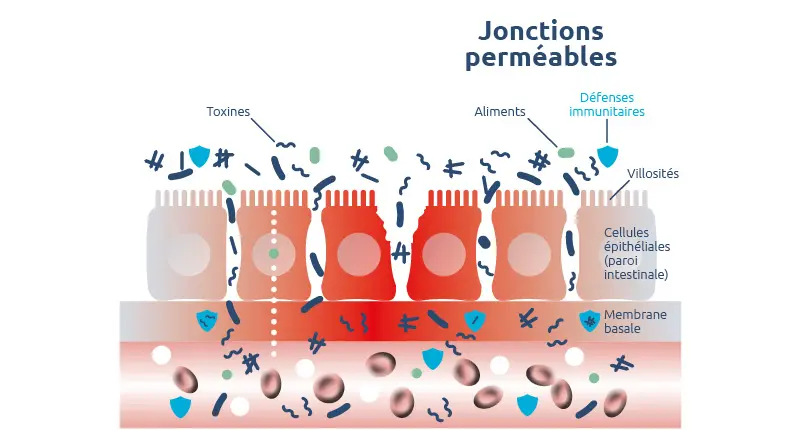
Mécanismes de l’hyperperméabilité
La prolifération de levures peut perturber les jonctions serrées entre les cellules de la muqueuse. Cette perméabilité accrue facilite alors le passage de molécules non digérées vers la circulation sanguine¹³. Cela peut stimuler des réactions immunitaires locales ou systémiques.
Dysbiose : quand la balance microbienne bascule
Un microbiote déséquilibré réduit les mécanismes de régulation naturels qui limitent d’ordinaire la croissance de Candida.
Interaction avec les jonctions serrées
Certaines substances produites par les levures peuvent affecter l’intégrité de la barrière épithéliale, contribuant à une perméabilité anormale.
Réaction défensive de la muqueuse
Face à cela, la muqueuse intestinale peut activer des processus de défense qui peuvent activer des réponses locales susceptibles de perturber l’équilibre de la muqueuse. Dans certains cas, cela peut être à l’origine d’une irritation persistante.
Candidose intestinale : quels signes observer ?
Manifestations digestives localisées
Les symptômes les plus courants incluent : ballonnements, alternance de transit, douleurs abdominales, ou encore gêne à la déglutition si l’œsophage est impliqué⁴. Une envie marquée pour les aliments sucrés est souvent rapportée⁵.
Retentissement général et manifestations systémiques
Certaines études suggèrent une association entre candidose chronique et fatigue persistante, troubles de l’humeur, ou sensibilité accrue aux allergènes⁶. Chez les patients immunodéprimés, une dissémination systémique est rare mais possible². Le lien bidirectionnel entre intestin et cerveau pourrait également être affecté, influençant potentiellement le bien-être émotionnel.
Approches naturelles pour rééquilibrer le microbiote
Une alimentation qui fait la différence
Réduire les apports en sucres rapides et privilégier une alimentation riche en fibres prébiotiques (comme la gomme d’acacia ou la farine de riz complet) favorise un environnement intestinal équilibré 5,⁸. Ces fibres nourrissent les bactéries bénéfiques et contribuent à abaisser le pH, conditions défavorables à l’expansion fongique.
Les plantes, un soutien traditionnel
Certaines plantes riches en composés phénoliques, comme l’origan à carvacrol, font l’objet d’un usage traditionnel dans le cadre du maintien de l’équilibre microbien⁹. Leur usage s’inscrit dans une approche globale encadrée.
Les enzymes digestives pour une digestion optimale
Les enzymes digestives participent à une meilleure assimilation des nutriments, ce qui peut limiter la présence de substrats fermentescibles dans le côlon.
Les nutriments, soutien de la barrière intestinale
Le zinc et la vitamine D contribuent au fonctionnement normal du système immunitaire et au maintien de la muqueuse ¹². Ces nutriments contribuent à maintenir l’intégrité de la barrière intestinale.
Les probiotiques, armée microscopique bénéfique
Certaines souches probiotiques bien documentées, comme Lactiplantibacillus plantarum 299v et Bifidobacterium longum BB536, occupent la même niche écologique que Candida albicans. Elles produisent de l’acide lactique, contribuant à un microbiote équilibré et au, comme démontré après 8 semaines de supplémentation¹⁰ ¹¹.
Approche intégrée pour le bien-être intestinal
Etape 1 : Recréer un terrain défavorable à Candida
La première étape consiste à adapter l’alimentation, réduire le stress et soutenir les fonctions digestives de base.
Etape 2 : Optimiser digestion et intégrité intestinale
Favoriser une bonne digestion et soutenir la barrière intestinale contribue à maintenir un écosystème équilibré
Etape 3 : Restaurer la diversité microbienne
La réintroduction de fibres prébiotiques et de probiotiques ciblés permet de renforcer la diversité du microbiote, élément central d’un équilibre durable.

En résumé
La candidose intestinale reflète un déséquilibre transitoire entre bactéries protectrices et levures opportunistes. Une approche globale, centrée sur l’hygiène de vie, la nutrition et le microbiote, peut favoriser le retour à un équilibre intestinal durable. Cette approche, accompagnée par un professionnel de santé, favorise un retour durable au bien-être digestif.
Références scientifiques
- Tong, Y., & Tang, J. (2017). Candida albicans infection and intestinal immunity. Microbiological Research, 198, 27–35. https://doi.org/10.1016/j.micres.2017.02.002
- Cornely, O. A., Sprute, R., Bassetti, M., Chen, S. C., Groll, A. H., Kurzai, O., Lass-Flörl, C., Ostrosky-Zeichner, L., Rautemaa-Richardson, R., Revathi, G., Santolaya, M. E., White, P. L., Alastruey-Izquierdo, A., Arendrup, M. C., Baddley, J., Barac, A., Ben-Ami, R., Brink, A. J., Grothe, J. H., Guinea, J., … Zhu, L. P. (2025). Global guideline for the diagnosis and management of candidiasis: an initiative of the ECMM in cooperation with ISHAM and ASM. The Lancet. Infectious Diseases, 25(5), e280–e293. https://doi.org/10.1016/S1473-3099(24)00749-7
- Pfaller, M. A., & Diekema, D. J. (2007). Epidemiology of invasive candidiasis: a persistent public health problem. Clinical Microbiology Reviews, 20(1), 133–163. https://doi.org/10.1128/CMR.00029-06
- R, A. N., & Rafiq, N. B. (2023, May 29). Candidiasis. In StatPearls. StatPearls Publishing. https://www.ncbi.nlm.nih.gov/books/NBK560624/
- Silva, S., Negri, M., Henriques, M., Oliveira, R., Williams, D. W., & Azeredo, J. (2011). Candida glabrata, Candida parapsilosis and Candida tropicalis: biology, epidemiology, pathogenicity and antifungal resistance. FEMS Microbiology Reviews, 36(2), 288–305. https://doi.org/10.1111/j.1574-6976.2011.00278.x
- Marano, G., Rossi, S., Sfratta, G., Traversi, G., Lisci, F. M., Anesini, M. B., Pola, R., Gasbarrini, A., Gaetani, E., & Mazza, M. (2025). Gut Microbiota: A New Challenge in Mood Disorder Research. Life, 15(4), 593. https://doi.org/10.3390/life15040593
- Tan, C. T., Xu, X., Qiao, Y., & Wang, Y. (2021). A peptidoglycan storm caused by β-lactam antibiotic’s action on host microbiota drives Candida albicans infection. Nature Communications, 12(1), 2560. https://doi.org/10.1038/s41467-021-22845-2
- Michel, C., Kravtchenko, T. P., David, A., Gueneau, S., Kozlowski, F., & Cherbut, C. (1998). In vitro prebiotic effects of Acacia gums onto the human intestinal microbiota depends on both botanical origin and environmental pH. Anaerobe, 4(6), 257–266. https://doi.org/10.1006/anae.1998.0178
- Yuan, X., Cao, D., Xiang, Y., Jiang, X., Liu, J., Bi, K., Dong, X., Wu, T., & Zhang, Y. (2024). Antifungal activity of essential oils and their potential synergistic effect with amphotericin B. Scientific Reports, 14, 31125. https://doi.org/10.1038/s41598-024-82380-0
- Arvidsson Nordström, E., et al. (2021). Lactiplantibacillus plantarum 299v (LP299V®): three decades of research. Beneficial Microbes, 12(5), 441–465. https://doi.org/10.3920/BM2020.0191
- Ejima, R., et al. (2024). The Impact of Fermented Milk Products Containing Bifidobacterium longum BB536 on the Gut Environment: A Randomized Double-Blind Placebo-Controlled Trial. Nutrients, 16(21), 3580. https://doi.org/10.3390/nu16213580
- DiGuilio, K. M., Rybakovsky, E., Abdavies, R., Chamoun, R., Flounders, C. A., Shepley-McTaggart, A., Harty, R. N., & Mullin, J. M. (2022). Micronutrient Improvement of Epithelial Barrier Function in Various Disease States: A Case for Adjuvant Therapy. International Journal of Molecular Sciences, 23(6), 2995. https://doi.org/10.3390/ijms23062995
- Zhai, B., Ola, M., Rolling, T., Tosini, N. L., Joshowitz, S., Littmann, E. R., Amoretti, L. A., Fontana, E., Wright, R. J., Miranda, E., Veelken, C. A., Morjaria, S. M., Peled, J. U., van den Brink, M. R. M., Babady, N. E., Butler, G., Taur, Y., & Hohl, T. M. (2020). High-resolution mycobiota analysis reveals dynamic intestinal translocation preceding invasive candidiasis. Nature Medicine, 26(1), 59–64. https://doi.org/10.1038/s41591-019-0709-7