Comment savoir si on est intolérant au gluten ?
L’intolérance au gluten est une problématique de plus en plus connue du grand public. Pourtant, elle reste mal diagnostiquée, en particulier lorsqu’elle ne relève pas de la forme la plus sévère : la maladie cœliaque. Environ 1 % des Français seraient atteints de cette pathologie auto-immune, mais plusieurs millions pourraient être sensibles au gluten sans le savoir1.
Comprendre les signes, les étapes de diagnostic et les leviers d’action permet de mieux gérer cette sensibilité alimentaire, souvent associée à des désagréments digestifs et à une altération du bien-être général.

Qu’est-ce que l’intolérance au gluten ?
L’intolérance au gluten est une maladie auto-immune qui se déclenche quand une personne mange des aliments contenant du gluten. Cette protéine se trouve naturellement dans certaines céréales comme le blé, l’orge et le seigle.
Contrairement à ce qu’on pourrait penser, ce n’est pas juste une « difficulté à digérer ». C’est beaucoup plus complexe : le système immunitaire de la personne se trompe d’ennemi et attaque l’intestin 1.
Elle peut se manifester sous deux formes distinctes :
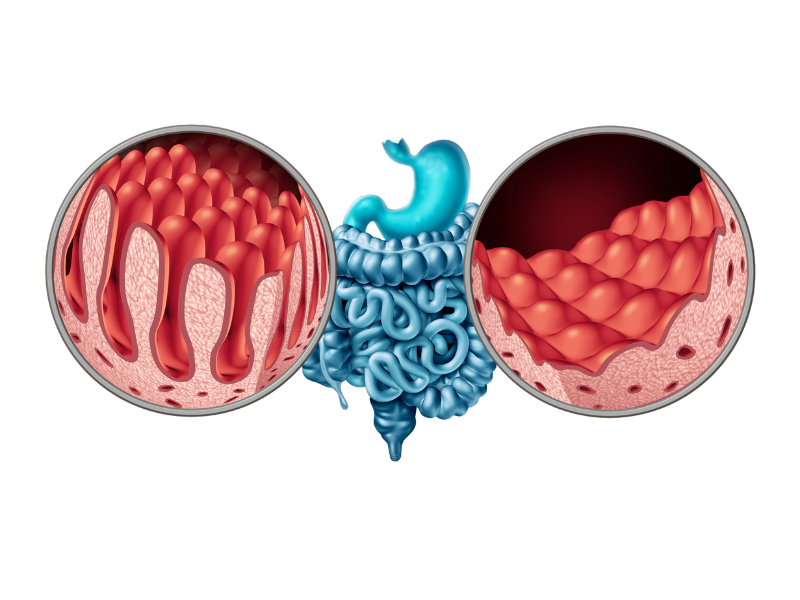
- La maladie cœliaque, qui correspond à une réponse auto-immune contre la paroi intestinale après ingestion de gluten. Elle entraîne des lésions de l’intestin grêle, affectant l’absorption des nutriments.
- L’hypersensibilité non cœliaque au gluten, qui provoque des symptômes similaires sans preuve biologique ou histologique de lésion intestinale.
Dans les deux cas, la consommation de gluten peut être à l’origine d’un inconfort digestif important, mais la gravité et la nature des mécanismes sous-jacents diffèrent.
Les symptômes de l’intolérance au gluten
L’intolérance au gluten peut s’exprimer par des signes digestifs ou extra-digestifs. Leur variété contribue souvent à retarder le diagnostic.
Les symptômes les plus fréquents sont :
- Troubles digestifs : ballonnements, flatulences, diarrhées fréquentes, transit irrégulier, inconfort abdominal.
- Manifestations générales : fatigue persistante, douleurs musculaires ou articulaires inexpliquées, maux de tête, irritabilité.
- Carences nutritionnelles : notamment en fer, calcium, magnésium ou vitamines B, liées à une absorption intestinale réduite en cas de maladie cœliaque.
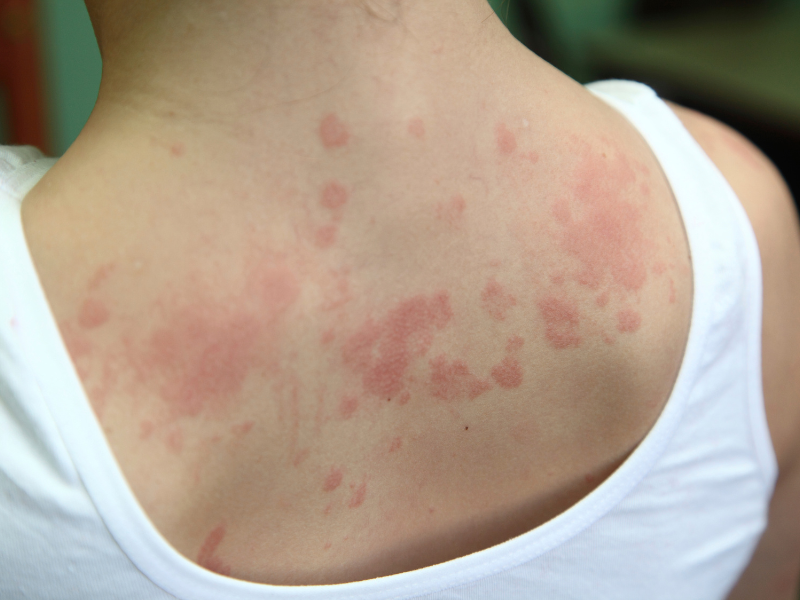
- Symptômes cutanés : démangeaisons ou éruptions, parfois associées à la dermatite herpétiforme.
On estime que près de 80 % des cas de maladie cœliaque restent non diagnostiqués, les signes étant souvent confondus avec d’autres troubles digestifs comme le syndrome de l’intestin irritable2.
Obtenir un diagnostic pour confirmer son intolérance au gluten
Avant toute éviction du gluten, un diagnostic médical rigoureux est essentiel. Celui-ci permet de distinguer la maladie cœliaque d’une sensibilité au gluten ou d’un autre trouble digestif.
Consulter un spécialiste : étape incontournable
Le premier réflexe doit être de consulter un médecin ou un gastro-entérologue. Ce professionnel :
– évalue les antécédents familiaux (la prédisposition génétique joue un rôle reconnu dans la maladie cœliaque),
– analyse les symptômes et leur lien avec la consommation de gluten,
– prescrit des examens adaptés, en suivant un protocole validé.L’autodiagnostic et l’arrêt du gluten sans avis médical risquent de fausser les résultats et compliquer le diagnostic.

Étapes du diagnostic médical
- Tests sanguins
La première étape repose sur des analyses biologiques à jeun. Les marqueurs recherchés sont :
-
- les anticorps anti-transglutaminases IgA, très spécifiques de la maladie cœliaque,
- les anticorps anti-endomysium (EMA), souvent utilisés en confirmation.
Un déficit en IgA peut aussi être recherché pour affiner l’interprétation. Ces tests permettent une forte suspicion, mais ne suffisent pas à eux seuls.
- Biopsie intestinale
Lorsque les tests sont positifs, une endoscopie digestive est proposée. Elle permet de prélever un fragment de la paroi intestinale pour :
-
- rechercher une atrophie des villosités, typique de la maladie cœliaque,
- mesurer l’intensité des lésions.
Cet examen reste la référence pour poser un diagnostic formel.
- Test d’éviction et de réintroduction
Dans le cas d’une hypersensibilité non cœliaque, les tests sont souvent négatifs. Le médecin peut alors proposer un test d’éviction : suppression du gluten pendant 4 à 6 semaines, puis réintroduction progressive. Une amélioration suivie d’une rechute permet de poser un diagnostic fonctionnel.
Attention : ce test doit impérativement être encadré par un professionnel. Supprimer le gluten avant les examens peut rendre impossible le diagnostic de la maladie cœliaque3.
Intolérance au gluten et déséquilibre du microbiote
L’exposition au gluten chez les personnes sensibles peut altérer l’intégrité de la barrière intestinale.
Une perméabilité accrue de la muqueuse digestive favorise le passage de molécules indésirables et perturbe la composition du microbiote intestinal(4). Ce déséquilibre, appelé dysbiose, est de plus en plus étudié.
Un microbiote affaibli peut aggraver l’inconfort digestif et réduire la production de métabolites bénéfiques comme le butyrate, essentiel au bon fonctionnement de la muqueuse5. Il est donc crucial, dans une stratégie globale de prise en charge, de soutenir la flore intestinale.
Le rôle des probiotiques dans le confort digestif
Certaines souches probiotiques ont été étudiées pour leur capacité à :
- favoriser la régulation de la perméabilité intestinale6,
- moduler la réponse immunitaire intestinale7,
- soutenir la digestion chez les personnes sensibles au gluten8.
Parmi les souches documentées, Lactobacillus rhamnosus GG et Bifidobacterium breve se distinguent par leur impact sur le confort intestinal, la modulation de la flore et l’amélioration de certains marqueurs de l’inflammation digestive9.
L’intégration de probiotiques dans l’alimentation ou sous forme de complément, en lien avec un professionnel de santé, peut ainsi contribuer au maintien de l’équilibre du microbiote en cas de sensibilité au gluten.

Comment mieux gérer son intolérance au gluten ?
Adopter un mode de vie adapté est essentiel pour préserver la qualité de vie.
Les recommandations générales incluent :
- une alimentation naturellement sans gluten, axée sur les fruits, légumes, légumineuses, pseudocéréales (quinoa, sarrasin) et protéines maigres,
- une vigilance sur les produits transformés et les contaminations croisées,
- le maintien d’un apport optimal en fibres et nutriments essentiels : fer, vitamine D, acide folique,
- la gestion du stress qui influence également la sensibilité intestinale10,
- un soutien ciblé du microbiote, sous encadrement professionnel.

En résumé
L’intolérance au gluten englobe à la fois la maladie cœliaque et l’hypersensibilité non cœliaque. Pour savoir si elle est réellement en cause, un diagnostic médical est indispensable. Ce parcours inclut des analyses biologiques, éventuellement une biopsie et parfois un test d’éviction contrôlé.
En parallèle, protéger son microbiote intestinal peut contribuer au maintien du confort digestif, notamment grâce à certaines souches probiotiques aux effets documentés.
Une alimentation adaptée, la réduction du stress et une approche globale du bien-être digestif permettent de mieux vivre avec une sensibilité au gluten.
Références scientifiques:
- Catassi, C., Bai, J. C., Bonaz, B., Bouma, G., Calabrò, A., Carroccio, A., Castillejo, G., Ciacci, C., Cristofori, F., Dolinsek, J., Francavilla, R., Elli, L., Green, P., Holtmeier, W., Koehler, P., Koletzko, S., Meinhold, C., Sanders, D., Schumann, M., Schuppan, D., … Fasano, A. (2013). Non-Celiac Gluten sensitivity: the new frontier of gluten related disorders. Nutrients, 5(10), 3839–3853. https://doi.org/10.3390/nu5103839
- Singh, P., Arora, A., Strand, T. A., Leffler, D. A., Catassi, C., Green, P. H., Kelly, C. P., Ahuja, V., & Makharia, G. K. (2018). Global Prevalence of Celiac Disease: Systematic Review and Meta-analysis. Clinical gastroenterology and hepatology : the official clinical practice journal of the American Gastroenterological Association, 16(6), 823–836.e2. https://doi.org/10.1016/j.cgh.2017.06.037
- Rubio-Tapia, A., Hill, I. D., Kelly, C. P., Calderwood, A. H., Murray, J. A., & American College of Gastroenterology (2013). ACG clinical guidelines: diagnosis and management of celiac disease. The American journal of gastroenterology, 108(5), 656–677. https://doi.org/10.1038/ajg.2013.79
- Conte, M., Porpora, M., Nigro, F., Nigro, R., Budelli, A. L., Barone, M. V., & Nanayakkara, M. (2021). Pro-Pre and Postbiotic in Celiac Disease. Applied Sciences, 11(17), 8185. https://doi.org/10.3390/app11178185
- De Palma, G., Nadal, I., Collado, M. C., & Sanz, Y. (2009). Effects of a gluten-free diet on gut microbiota and immune function in healthy adult human subjects. The British journal of nutrition, 102(8), 1154–1160. https://doi.org/10.1017/S0007114509371767
- Ríos-Covián, D., Ruas-Madiedo, P., Margolles, A., Gueimonde, M., de Los Reyes-Gavilán, C. G., & Salazar, N. (2016). Intestinal Short Chain Fatty Acids and their Link with Diet and Human Health. Frontiers in microbiology, 7, 185. https://doi.org/10.3389/fmicb.2016.00185
- Nylund, L., Satokari, R., Salminen, S., & de Vos, W. M. (2014). Intestinal microbiota during early life – impact on health and disease. The Proceedings of the Nutrition Society, 73(4), 457–469. https://doi.org/10.1017/S0029665114000627
- Smecuol, E., Hwang, H. J., Sugai, E., Corso, L., Cherñavsky, A. C., Bellavite, F. P., González, A., Vodánovich, F., Moreno, M. L., Vázquez, H., Lozano, G., Niveloni, S., Mazure, R., Meddings, J., Mauriño, E., & Bai, J. C. (2013). Exploratory, randomized, double-blind, placebo-controlled study on the effects of Bifidobacterium infantis natren life start strain super strain in active celiac disease. Journal of clinical gastroenterology, 47(2), 139–147. https://doi.org/10.1097/MCG.0b013e31827759ac
- Olivares, M., Neef, A., Castillejo, G., Palma, G. D., Varea, V., Capilla, A., Palau, F., Nova, E., Marcos, A., Polanco, I., Ribes-Koninckx, C., Ortigosa, L., Izquierdo, L., & Sanz, Y. (2015). The HLA-DQ2 genotype selects for early intestinal microbiota composition in infants at high risk of developing coeliac disease. Gut, 64(3), 406–417. https://doi.org/10.1136/gutjnl-2014-306931
- Chitkara, D. K., van Tilburg, M. A., Blois-Martin, N., & Whitehead, W. E. (2008). Early life risk factors that contribute to irritable bowel syndrome in adults: a systematic review. The American journal of gastroenterology, 103(3), 765–775. https://doi.org/10.1111/j.1572-0241.2007.01722.x